
Cách viết phương trình điện li
Chúng tôi xin giới thiệu bài Cách viết phương trình điện li được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy môn Hóa học lớp 11. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh.
Lưu ý: Nếu bạn muốn Tải bài viết này về máy tính hoặc điện thoại, vui lòng kéo xuống cuối bài viết.
1. Chất điện li mạnh
Chất điện li yếu là chất mà khi tan trong nước, các phân tử hòa tan đều phân li ra ion. Chúng ta cùng tìm hiểu một số phương trình điện li của các chất điện li mạnh đặc trưng dưới đây:
+) Axit: HCl, H2SO4 , HNO3 …
HCl → H+ + Cl-
H2SO4 → 2H+ + SO4
+) Bazo: NaOH, Ca(OH)2 …
NaOH → Na+ + OH-
Ca(OH)2 → Ca2+ + 2OH-
+) Muối: NaCl, CaCl2 , Al2(SO4)3
NaCl → Na+ + Cl-
CaCl2 → Ca2+ + 2Cl-
Al2(SO4)3 → 2Al3+ + 3SO4
2. Chất điện li yếu
Ngược lại với chất điện li mạnh thì chất điện li yếu là chất mà khi chúng được hòa tan trong nước, sẽ có một số ít phần từ hòa tan phân li ra ion, phần còn lại vẫn tồn tại dưới dạng phần tử trong dung dịch.Các chất điện li yếu thường gặp là: axit yếu, bazơ yếu, các muối không tan, muối dễ bị phân hủy,..
Ví dụ: HF, H2S, H2SO3, CH3COOH, NH3, Fe(OH)2, Cu(OH)2, AgCl, PbSO4… Và đặc biệt H2O là một chất điện li yếu.
Phương pháp giải bài tập phương trình điện li
Dạng 1: Chất điện li mạnh
Bước 1: Viết phương trình điện li của chất điện li mạnh
Dựa vào bảng phương trình trên cùng với dữ kiện đề bài, ta thiết lập một số phương trình liên quan đến các chất có trong đề bài. Một trong những chất điện li mà chúng ta khá hay quên đó chính là H2O. Đây là bước cực kì quan trọng quyết định trực tiếp đến kết quả tính toán của bài tập.
Bước 2: Xác định nồng độ mol của ion
- Tính số mol của chất điện li có trong dung dịch
- Viết phương trình điện li chính xác, biểu diễn số mol lên các phương trình điện li đã biết
- Tính nồng độ mol của ion
Ví dụ: Hòa tan 12,5 gam tinh thể CuSO4.5H2O trong nước thành 200 ml dung dịch. Tính nồng độ mol các ion trong dung dịch thu được .
Lời giải:
a.) nCuSO4. 5H2O = 12,5/250 = 0,05 (mol)
CuSO4.5H2O → Cu2+ + SO4 2- + 5H2O
0,05 0,05 0,05 (mol)
[ Cu2+] = [SO42-] = 0.05/0.2 = 0.25M
Dạng 2: Định luật bảo toàn điện tích
Bước 1: Phát biểu định luật
Trong một dung dịch chứa hoàn toàn các chất điện li, thì tổng số mol của điện tích âm luôn bằng tổng số mol của điện tích dương. (Luôn luôn bằng nhau)
Ví dụ: Dung dịch A chứa Na+ 0,1 mol , Mg2+ 0,05 mol , SO4 2- và 0,04 mol còn lại là Cl- . Tính khối lượng muối trong dung dịch.
Giải: Vẫn áp dụng các công thức trên về cân bằng điện tích ta dễ dàng tính được khối lượng muối trong dung dịch là: m = 11.6 gam.
Dạng 3: Bài toán về chất điện li
Bước 1: Viết phương trình điện li
Như chúng ta đã tìm hiểu cách viết phương trình điện li rất chi tiết ở phía trên. Ở đây chúng ta không cần nêu lại nữa mà tiến hành sang bước 2 đó là …
Bước 2: Xác định độ điện li
Áp dụng công thức độ điện li dưới đây nhé:
Sau đó sử dụng phương pháp 3 dòng thật hiệu quả:
Biến số anla có thể quyết định nó là chất điện li mạnh, yếu hay là chất không điện li. Cụ thể là:
- α = 1: chất điện li mạnh
- 0 < α < 1: chất điện li yếu
- α = 0: chất không điện li
Ví dụ: Điện li dung dịch CH3COOH 0,1M được dung dịch có [H+] = 1,32.10-3 M. Tính độ điện li α của axit CH3COOH.
Lời giải: Bài tập này khá đơn giản và được trích trong sách chinh phục hóa hữu cơ của Nguyễn Anh Phong. húng ta làm như sau với ghi nhớ rằng đề bài cho chất điện li và đã có nồng độ nên mới theo hướng dưới đây:
Dạng 4: Xác định hằng số điện li
Để làm bài toán này ta chia thành các bước như sau: Xác định hằng số của axit và xác định hằng số điện li của bazơ
Ví dụ: Tính nồng độ mol ion H+ của dung dịch CH3COOH 0,1M, biết hằng số phân li của axit Ka = 1,75.10-5.
==> Đề bài khá đơn giản khi cho biến đầy đủ dữ kiện, đề bài không quá lách léo và ta phải thực hiện như sau để tính được nồng độ ion H+:
Dạng 5: Tính độ PH dựa vào nồng độ H+
Bước 1: Tính độ Ph của Axit
- Tính số mol axit điện li axit
- Viết phương trình điện li axit
- Tính nồng độ mol H+ sau đó suy ra nồng độ mol của PH bằng mối liên hệ giữa hai nồng độ này qua hàm log.
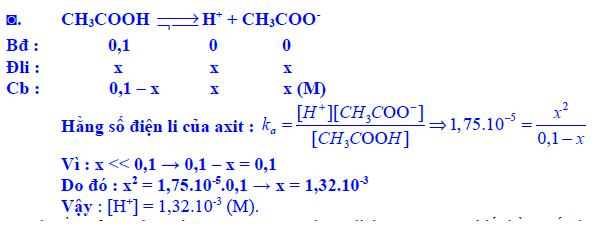
Bước 2: Xác định độ PH của baz ơ
Ta thực hiện theo các bước sau:
- Tính số mol bazơ của điện li
- Viết phương trình điện li bazơ
- Tính nồng độ mol OH- rồi suy ra [H]+
- Tính độ PH
Ví dụ 1: Tính pH của dung dịch chứa 1,46 gam HCl trong 400 ml .
Ví dụ 2: Tính pH của dung dịch chứa 0,4 gam NaOH trong 100 ml .
Ví dụ 3: Tính pH của dung dịch tạo thành khi trộn 100 ml dung dịch HCl 1M với 400 ml dung dịch NaOH 0,375 M
Lời giải cho các bài tập trên
Ví dụ 1:
nHCl = 0,04 (mol)
HCl → H+ + Cl-0,04 0,04 (mol) .[H+] = 0,04/0,4 = 0,1 (M).
pH = - lg[H+] = 1.
Ví dụ 2:
nNaOH = 0,4/40 = 0,01 (mol) .
NaOH → Na+ + OH- . 0,01 0,01 (mol) . [OH-] = 0,01/0,1 = 0,1 (M) .
Ta có: [H+].[OH-] = 10-14 → [H+] = 10-13 → pH = 13 .
Ví dụ 3: Đáp số pH = 13.
Dạng 6: Xác định nồng độ mol dựa vào độ pH
Bài toán trải qua hai quá trình tính nồng độ mol của axit và nồng độ mol của bazơ. Và lưu ý một số điểm như sau:
- pH > 7: môi trường bazo.
- pH < 7: môi trường axit.
- Ph = 7: môi trường trung tính.
Dạng 7: Axit, bazo và sự lưỡng tính theo hai lý thuyết
Đây là một dạng toán khá ít gặp tuy nhiên các em cần nắm vững hai lý thuyết A - rê - ni - ut về sự điện li và thuyết Bron - stêt về thuyết proton. Hai thuyết này có sự định nghĩa hoàn toàn khác nhau về thế nào là chất bazơ và thế nào là chất axit.
Ví dụ:
Trong các phản ứng dưới đây, ở phản ứng nào nước đóng vai trò là một axit, ở phản ứng nào nước đóng vai trò là một bazơ (theo Bron - stêt).
- HCl + H2O → H3O++ Cl-
- Ca(HCO3)2→ CaCO3+ H2O + CO2 .
- CuSO4+ 5H2O → CuSO4.5H2O .
Lời giải:
HCl → H++ Cl-
H2O + H+ → H3O+
Do đó H2O nhận proton H+ nên thể hiện tính bazơ .
NH3+ H+OH → NH4+
Do đó H2O nhường proton H+ nên thể hiện tính axit.
-
Như vậy VnDoc đã giới thiệu các bạn tài liệu Cách viết phương trình điện li. Mời các bạn tham khảo thêm tài liệu: Giải bài tập Hóa học lớp 11, Giải SBT Hóa Học 11, Trắc nghiệm Hóa học 11, Tài liệu học tập lớp 11
Link nội dung: https://appstore.edu.vn/cach-viet-phuong-trinh-dien-li-a68917.html